1.成果名称及简介
(1)成果名称:Incyclinide协同黏菌素在制备携带mcr基因的肠杆菌科细菌的杀菌药物中的应用
(2)成果关键词:肠杆菌科细菌、Incyclinide、黏菌素、mcr基因、杀菌药物
(3)成果简介:
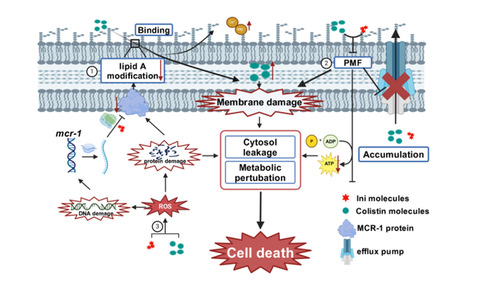
本发明公开了一种Incyclinide协同黏菌素在制备携带mcr基因的肠杆菌科细菌的杀菌药物中的应用。Incyclinide(Ini)是一种经过化学修饰的四环素衍生物,本发明证明了Ini在体外和动物模型中能够恢复黏菌素对携带mcr基因的肠杆菌科细菌的杀菌效果,机制分析显示,Ini通过抑制脂质A修饰、诱导氧化损伤以及消散质子动力(PMF),来恢复黏菌素的药效。Ini作为一种黏菌素佐剂,在对抗携带mcr基因的肠杆菌科细菌方面具有巨大的潜力。
2.知识产权情况
(1)知识产权类型
☑专利 □软著 □技术秘密 □植物新品种 □集成电路布图设计 □其他:
(2)具体清单:
成果名称:Incyclinide协同黏菌素在制备携带mcr基因的肠杆菌科细菌的杀菌药物中的应用
专利号:202510379597.3
申请时间:2025年03月28日
授权时间:在审
发明人:董宁,许晨
权利人:浙江大学
3.技术领域/行业分类
技术领域:生物医药、抗感染药物研发、抗生素增效剂(佐剂)技术、微生物耐药性防控
行业分类:医药制造业(C27)、生物技术产业、创新药研发(Pharma R&D)
4.行业/产业现状和专利布局
当前,全球面临严峻的抗生素耐药性危机,但新型抗生素研发进展缓慢、成本高昂,市场亟需创新解决方案。现有专利布局主要集中在β-内酰胺酶抑制剂类佐剂(如与青霉素、头孢菌素联用的克拉维酸、他唑巴坦及其新型衍生物),以及探索破坏细菌生物膜、增强药物渗透或靶向递送等新机制的佐剂技术,整体呈现由传统化学增效向多机制联合、精准化设计发展的趋势。
5.技术/行业痛点
抗生素开发行业面临研发成本高、周期长、科学突破难与市场回报低的尖锐矛盾,导致企业研发动力不足;同时,严格的监管政策、激烈的市场竞争、原材料波动及公众滥用问题进一步加剧了产业困境,其核心痛点在于重大公共卫生需求与商业利益失衡所致的“市场失灵”。
6.解决方案与技术优势
技术领域
本发明属于杀菌药物开发技术领域,尤其涉及一种Incyclinide协同黏菌素在制备携带mcr基因的肠杆菌科细菌的杀菌药物中的应用。
背景技术
抗生素在医疗领域的广泛应用大大降低了与感染相关的死亡率和发病率,为医疗保健带来了革命性的变化。但是,抗生素在人类医疗和农业中的过度使用和滥用已经造成了选择压力,促进了耐药细菌的广泛传播,这大大加剧了抗生素耐药性(AMR)危机的不断升级。抗生素耐药不仅威胁着个体患者的健康,还构成了一场可能逆转数十年医学进步的全球健康危机,这凸显了由世界卫生组织领导的全球协调行动的迫切需求。近年来,抗生素耐药性迅速蔓延,尤其是对最后一线抗生素,如黏菌素、替加环素、碳青霉烯类和头孢烯醇的耐药性。
黏菌素(也称为多黏菌素E)是一种多肽类阳离子抗生素,对大多数革兰阴性病原体显示出显著的抗菌活性,特别是对铜绿假单胞菌(Pseudomonas aeruginosa)、鲍曼不动杆菌(Acinetobacter baumannii)、肺炎克雷伯菌(Klebsiella pneumoniae)和大肠埃希菌(Escherichia coli)。对于这些细菌种类,一旦表现出多药耐药性,黏菌素往往成为唯一的有效抗生素选项。黏菌素通过静电作用与革兰阴性病原体外膜中的脂多糖(LPS)的阴离子脂质A残基结合,从而发挥其抗菌效果。这种结合导致细胞膜通透性增加、细胞内容物泄漏,最终引发溶解性细胞死亡。然而,黏菌素的临床应用受到其副作用的显著限制,尤其是肾毒性和神经毒性,同时还受到病原体中迅速出现和传播的耐药机制的影响。黏菌素耐药性的获得主要是由于黏菌素与脂质A的负电荷残基之间的静电相互作用减少所致。这一过程通常是由阳离子取代基(如磷酸乙醇胺(pEtN)或4-氨基-4-脱氧-L-阿拉伯糖基团)结合到LPS脂质A成分的磷酸基团上所介导的。这种修饰是由相应的转移酶 EptA 和 ArnT 催化的,从而减少了细菌细胞表面的整体负电荷。之前,这些LPS修饰被认为由激活两组分调控系统PhoP-PhoQ和PmrA-PmrB的染色体突变所导致,这些系统调控eptA或arnT的表达。由于染色体黏菌素耐药性的传播有限,其临床影响主要局限于暴发事件。然而,通过质粒水平转移可移动的黏菌素耐药(mcr)基因已被确认为一种关键机制,促进了耐药性在同一物种内以及不同物种间的快速传播。耐多药菌株,尤其是那些携带对其他最后一线抗生素耐药基因的菌株,可能与mcr基因共存, 这种基因共存的趋势对临床治疗构成了严峻挑战,因为它可能导致现有抗生素治疗方案失效,并加速有效抗生素资源的耗竭。
利用佐剂开发新的治疗策略,以恢复耐药细菌对现有抗生素的敏感性,是一种有望延长经过充分研究和临床验证的药物使用寿命的方法。目前在临床使用的协同疗法中,一个突出的例子是将β-内酰胺类抗生素与β-内酰胺酶抑制剂联合使用。除了使用针对抗药性基因编码的特定蛋白质的抑制剂外,利用佐剂抑制关键通路也能恢复抗生素的效力。例如,研究发现天然类黄酮可以通过干扰细菌的铁平衡来恢复黏菌素的效力。然而,目前尚无可用于临床的商业化黏菌素佐剂,这突出表明了开发潜在黏菌素佐剂的紧迫需求。
发明内容
为克服现有技术的缺点和不足,本发明的目的在于提供一种Incyclinide协同黏菌素在制备携带mcr基因的肠杆菌科细菌的杀菌药物中的应用。
本发明是这样实现的,Incyclinide协同黏菌素在制备携带mcr基因的肠杆菌科细菌的杀菌药物中的应用。
本发明克服现有技术的不足,提供一种Incyclinide协同黏菌素在制备携带mcr基因的肠杆菌科细菌的杀菌药物中的应用。Incyclinide(Ini)是一种经过化学修饰的四环素衍生物,本发明证明了Ini在体外和动物模型中能够恢复黏菌素对携带mcr基因的肠杆菌科细菌的杀菌效果,机制分析显示,Ini通过抑制脂质A修饰、诱导氧化损伤以及消散质子动力(PMF),来恢复黏菌素的药效。Ini作为一种黏菌素佐剂,在对抗携带mcr基因的肠杆菌科细菌方面具有巨大的潜力优选地,所述肠杆菌科细菌包括大肠埃希菌P47 、大肠埃希菌P80。相比于现有技术的缺点和不足,本发明具有以下有益效果:本发明通过体外实验、斑马鱼感染模型和小鼠感染模型证明,Incyclinide(Ini)与黏菌素协同作用,可消灭携带 mcr 的肠杆菌科细菌。机理研究表明,Ini 通过抑制 mcr 的表达来抑制脂质 A 的修饰,从而促进黏菌素进入细菌细胞膜。此外,Ini 还会耗散质子动力(PMF),从而损害依赖 PMF 的外排泵的功能,导致黏菌素在膜内积聚。积聚的黏菌素会诱发氧化应激,加剧膜损伤,最终导致细胞死亡。因此,Ini 具有成为一种高效黏菌素佐剂的巨大潜力,能够有效应对由携带mcr基因的病原体引发的感染所带来的日益严重的威胁。
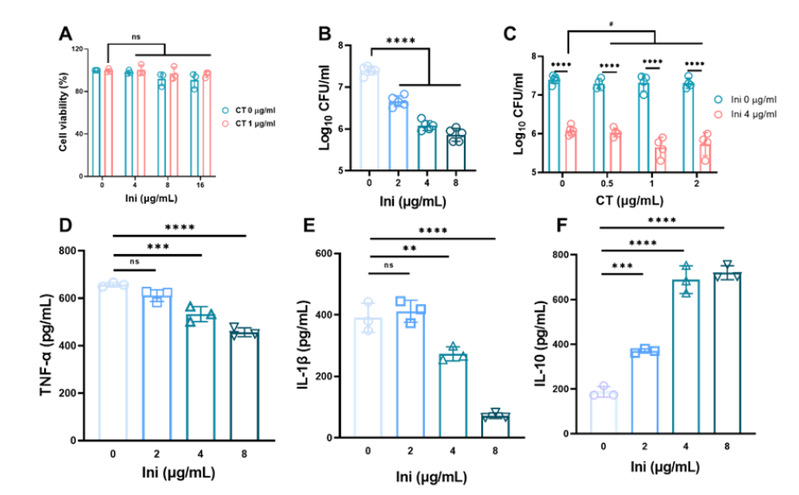
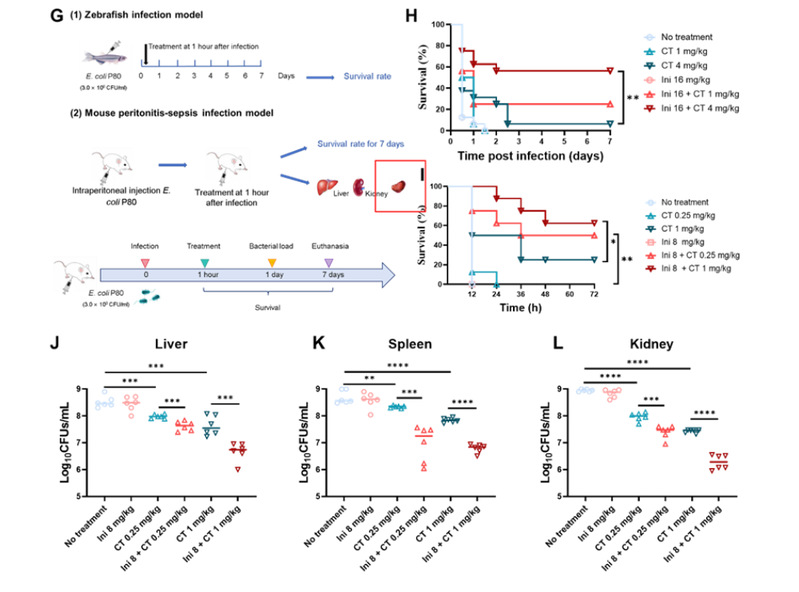
8.课题资助与所获奖励
(1)课题项目:
1.浙江省自然科学基金探索项目(Incyclinide恢复mcr-1阳性肠杆菌科细菌对黏菌素敏感性的作用机制研究,项目编号:LMS25C010002)
2. 国家重点研发计划课题(非洲重点地区结核病诊疗与综合防控策略研究,课题编号:2024YFC2310905)
9.技术成熟度:
□构思 ☑研发 □样品 ☑小试 □中试 □产业化、推广 □其他:
10.应用前景
(1)适用领域:抗菌药物研发
(2)目标客户:医疗系统、药企、政府部门等
(3)消费群体:临床及社区感染性病患
(4)商业计划及市场前景:本专利提供一种可显著增效抗生素、克服细菌耐药性并降低用药剂量的新型佐剂,有效解决行业研发成本高、临床疗效下降及商业回报不足等核心痛点。拟通过技术授权或联合开发模式,与具备成熟抗生素管线的制药企业合作,共同开发“抗生素+佐剂”复方产品,加速成果转化并共享收益。该技术顺应全球应对抗微生物耐药(AMR)的战略需求,符合各国政策支持方向,具备显著的临床价值与商业潜力,市场前景广阔。
11.合作转化方式
☑普通许可 ☑排他许可 ☑独占许可 ☑转让 ☑作价入股
☑技术开发 ☑技术咨询 ☑技术服务 □其他:
12.意向合作方
☑国有企业 ☑上市公司 ☑行业龙头企业 □其他:
13.意向合作金额
☑10万—50万 □50万—100万 □100万—500万
□500万—1000万 □1000万以上 □其他金额: □ 面议
14.科研团队
(1)项目负责人:姓名 董宁 ,职务职级 研究员
(2)主要成员:姓名 李阿慧 ,职务职级 无 ……
(3)科研团队的简介
科研团队依托浙江大学,该单位在医学、生命科学及交叉学科领域具有深厚的学术积淀、雄厚的科研实力和广泛的国际影响力。申请人所在学院为浙江大学医学院,长期聚焦聚焦新型抗菌药物靶点发现及抗生素佐剂的开发及应用。近年来,申请人已在相关领域发表SCI论文80余篇,其中以第一或通讯作者(含共同)身份发表40余篇,多篇代表性成果发表于 The Lancet Microbe、The Lancet Infectious Diseases、Nature Communications、EBioMedicine 和 Drug Resistance Updates 等国际权威期刊,部分研究被领域内顶级期刊作为亮点评述,受到国际同行广泛关注与高度评价。
15.联系方式
浙大工研院成果转化服务中心,0571-88982927。